行业观察|Biotech“探路”NPP计划,解锁走向海外又一路径
段静远/文
在国际上已经获批的创新药,要想尽早实现多地商业化,获得全球定价,是近几年摆在众多Biotech公司面前的一道考题。
常规操作下需要”先上市后入市”,然而海外上市路途漫漫,不确定性加剧,想要尽早在当地市场获批并非易事,事实是,打开市场,实现商业化的道路不止一条,打开更多通路也可以通向“罗马”。
博鳌乐城“先行先试”通道日渐被国内市场熟悉和了解,“乐城模式”旨在通过创新引进海外已经上市但尚未在国内上市的药品,让临床有急需且有一定支付能力的患者能够最快用到国际上已经获批且有定价的治疗方案。“乐城模式”成为目前跨国药企的药物或是国内企业license-in产品已在海外上市,进入国内市场的一条新通道。
日前,亚盛医药和供药解决方案的服务商Tanner Pharma合作,启动指定患者药物使用计划(Named Patient Program,NPP)。
NPP开始走进国内市场的“视野”。这次的合作也可以看作一个新例证,打开国内药企走向海外市场的思路和通道。
“首先是让临床急需的病人用上药。另一方面,对于企业来说,可以在进入海外市场时‘两条腿走路’,既可以走常规的完成临床试验后申报上市,也可以通过NPP的模式。而在NPP的模式下,通过商业化定价,更早更快获得商业收入,也可以通过真实世界数据缩短上市时间”,亚盛医药董事长、CEO杨大俊对财经网解读称。
NPP并非“新事物”,覆盖范围也不仅局限在一个国家或者区域。以这次亚盛医药这次的合作为例,该项目将在奥雷巴替尼尚未获得上市许可的区域为指定患者提供使用该药物的机会,计划覆盖130多个国家和地区。
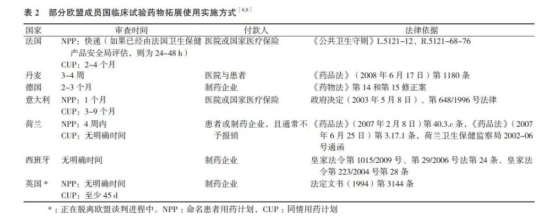
财经网注意到,以欧盟为例。中国新药与临床杂志2020年5月的期刊显示,2007年,EMA 人用药品委员会(Committee for Medicinal Products for Human Use,CHMP)发布《医疗产品同情使用指南》提出,部分成员国允许医生为患者提出临床试验药物拓展使用,即命名患者用药计划(Named Patient Programme,NPP)。
NPP计划下,医生基于临床治疗需要,为少数特定患者提出参加拓展用药计划的申请,并由医生作为项目责任主体,承担相应责任,通常参与患者数较少并在申请时明确用药患者的个人信息。
能够纳入NPP计划,对产品有哪些要求?
杨大俊告诉财经网,第一,关键是临床价值,要能满足当地患者尚未被满足的临床需求,医生愿意开具处方;第二,需要是药物已经在一国获批上市,证明安全有效。
作为“走出去”的一条通道,一定程度上与国内“引进来”的“乐城模式”具有“神似”。
“NPP和博鳌乐城模式都有这样的要求和路径,过去没有乐城模式,通过药监局获批是唯一的路径,目前打通了这条路径,可以两条腿走路”,杨大俊谈到。
在全世界范围内, 实现商业化的路径,最主要的是通过临床试验,获批上市后进入市场销售。以亚盛医药的奥雷巴替尼为例,于2019年开始在美国进行桥接临床试验,已经获得孤儿药资格认证、快速通道资格等,据杨大俊告诉财经网,目前临床研究都在继续推进。
财经网注意到,落地海南博鳌前,德琪医药的选择性核输出抑制剂塞利尼索,在落地博鳌乐城前,在中国香港地区开展了指定患者药物使用计划(NPP)。
据杨大俊指出,NPP目前已经开始被越来越多的企业接受,甚至有跨国药企在部分地区仅采用NPP计划,不再另外进行临床试验或者注册上市。“这些公司判断这样的方式可以满足当地患者的临床需求,达到商业化的目的。”
由于NPP不同于慈善赠药项目,需要患者自费购药企业药品定价和患者购药报销成为一个需要考量的问题。
以这次计划下的奥雷巴替尼为例,杨大俊告诉财经网,国际市场定价是按照国际的定价体系原则来做的,在咨询了合作方之后,奥雷巴替尼在NPP计划下的定价高于全球首个上市的三代BCR-ABL抑制剂普纳替尼(ponatinib)。“鉴于与普纳替尼相比,奥雷巴替尼体现出更优的安全性,另一方面,由于奥雷巴替尼还能满足目前市场尚未满足的临床需求。”
对应需要解决的就是支付问题。杨大俊告诉财经网,“每个国家不一样,在一部分的国家通过NPP可以报销,当地保险医保商保也是可以报销的。”
据上述提到的中国新药与临床杂志2020年5月刊文指出,仍以欧盟为例,对于拓展用药期间患者使用药物的费用承担及是否报销的问题,欧盟没有统一规定,不同的国家有不同的做法,大部分国家如德国、西班牙、英国、奥地利、希腊等是由制药企业免费提供的,法国、意大利由医院或国家医疗保险承担,荷兰则由患者或企业承担且通常不予报销。
财经网梳理注意到,匹配海外进口特药引进国内,就在2020年8月,全球首款境内外特种药品费用补偿型医疗保险产品“乐城特药险”正式发布,而后在2021年8月,乐城特药首次走出海南纳入普惠医保。
对于药企而言,无论是积极借助博鳌乐城作为进入国内市场的新通道,还是借由NPP计划实现出海,在较早实现商业化落地外,另一个重要意义在于实现“从临床研究到真实世界验证”。
信息显示,依托乐城先行区真实世界数据应用试点工作这一“快车道”,目前已有8个国际创新药械产品加速获批上市。海外上市新药要想拿到进入国内市场的“入场券”,通常需要开展三期临床试验,这一过程可能需要持续数年时间。以EyePoint公司氟轻松玻璃体内植入剂数据为例,通过博鳌先行先试,提前获得国家药品监督管理局的上市批复,商业化进程缩短约1年半。
真实世界研究也不仅局限在上市前,也会贯穿药械全生命周期监测评价。
国家药监局海南真实世界数据研究与评价重点实验室主任孙鑫曾指出,“除了帮助缩短药械临床研发进程,真实世界研究还可以促进中医药、罕见病、儿童和其他特殊人群药品的研发和临床评价,有利于开展药械全生命周期监测评价。”
在NPP计划下,财经网注意到,伊布替尼此前开展的一项全球大型真实世界研究指定患者项目,纳入来自30个国家的2908例复发难治CLL患者,通过与RESONATE临床研究结果对比,评估真实世界中复发难治CLL患者应用伊布替尼治疗的疗效与安全性。
 【作者:段静远】
(编辑:段静远) 关键字:
【作者:段静远】
(编辑:段静远) 关键字: 
